Apakah itu unsur nitrogen? Artikel ini akan membincangkan sifat, sejarah penghasilan nitrogen dan kegunaannnya dalam kehidupan seharian kita
Pengenalan
Nitrogen adalah unsur bukan logam yang berada dalam kumpulan 15 jadual berkala. Ia tidak mempunyai rasa, bau dan warna dan merupakan gas yang paling banyak berada di ruang atmosfera bumi dengan jumlah kira-kira 78% atau kira-kira 4000 trillion tan seterusnya menjadi unsur yang paling banyak yang membentuk dan memberi fungsi dalam kehidupan.
Ia adalah komponen asas dari semua protein dan boleh didapati dalam sistem kehidupan. Nitrogen di dalam air dan tanah boleh didapati dalam bentuk nitrat dan nitrit yang merupakan bahagian daripada kitaran nitrogen dan saling berkait antara satu sama lain.
Nitrogen penting dalam kehidupan kerana ia merupakan asas kepada pembentukan DNA yang merupakan tempat tersimpannya kod genetik. Contoh sebatian nitrogen banyak terdapat dalam bahan organik, makanan, baja, bahan letupan dan racun. Selain itu nitrogen bebas pula terdapat pada meteorit, gas gunung berapi, kawasan perlombongan, kolam air panas, matahari, nebula dan bintang.
Sifat utama Nitrogen
- Nombor atom: 7
- Berat atom: 14
- Kumpulan: 15
- Takat lebur: -210°C
- Takat didih: -195.8°C
- Ketumpatan: 0.001145 g cm−3
Sejarah Penghasilan
Unsur nitrogen telah ditemui oleh seorang doktor dan ahli kimia di Scotland, Daniel Rutherford pada tahun 1772 semasa menyiapkan tesisnya. Nitrogen diperolehi dari udara melalui proses yang dikenali sebagai pengasingan sulingan.
Dia mengeluarkan gas oksigen dan gas karbon dioksida dari udara dan lebihan gas tersebut didapati tidak menyokong proses pembakaran atau organisma hidup. Pada tahun 1760, beberapa orang Saintis terlebih dahulu mengkaji gas nitrogen seperti Henry Cavendish dan Joseph Priestley.
Apabila mereka mengeluarkan gas oksigen dari udara dan masukkan ia ke dalam tabung ujikaji mereka mendapati gas tersebut dapat memadamkan lilin yang menyala serta seekor tikus yang hidup di dalamnya segera mati. Walaubagaimanapun mereka tidak dapat mengenal pasti bahawa unsur itu adalah gas nitrogen. Mereka hanya menggelarkan ia sebagai udara yang tidak sempurna atau udara tanpa oksigen.
Nama nitrogen berasal dari bahasa Latin nitrium dan Greek nitron yang bermaksud soda dan gen yang membentuk. Nama itu telah diberikan oleh ahli kimia Perancis Jean-Antoine-Claude pada tahun 1790. Dia menjelaskan dengan lebih lanjut peranan gas tersebut yang tidak menyokong kehidupan seterusnya menyangah pandangan teori phlogiston yang popular pada abad ke-18.
Sifat kereaktifan
Nitrogen adalah gas yang tidak aktif pada suhu persekitaran dan tidak bergabung dengan oksigen, hidrogen dan kebanyakan unsur lain.
Walaubagaimanapun nitrogen boleh bergabung dengan oksigen dengan kehadiran kilat atau percikan api. Penghasilan tenaga elektrik daripada salah satu sumber berikut menyebabkan nitrogen dan oksigen membentuk nitrik oksida.
Nitrik oksida pula lebih aktif daripada nitrogen bebas. Sebagai contoh apabila nitrik oksida bergabung dengan oksigen dan air di udara maka ia akan membentuk asid nitrik. Semasa hujan, asid nitrik mendap ke dalam lapisan kerak bumi lalu bergabung dengan logam yang berada dalam kerak bumi maka akan menghasilkan sebatian yang dipanggil sebagai nitrit (NO2−) dan nitrat (NO3−).
Perubahan unsur nitrogen kepada sebatian nitrogen dipanggil sebagai fiksasi nitrogen. Tindak balas antara antara nitrogen dan oksigen di udara adalah contoh tindak balas fiksasi nitrogen. Terdapat sejenis bakteria yang hidup dalam akar tumbuhan yang mengubah nitrogen di udara dan menukarkannya menjadi ammonium (NH4+).
Bakteria lain pula akan menukarkan ammonium tersebut kepada sebatian nitrit kemudian nitrat yang akhirnya menghasilkan molekul protein serta asid amino yang penting untuk perkembangan dan pertumbuhan sel organisma hidup.
Haiwan akan memakan tumbuhan yang mengandungi protein tersebut dan akhirnya sebatian nitrogen kembali semula ke dalam tanah melalui bahan buangan haiwan dan bangkai yang terurai apabila ia mati. Bakteria akan menukar hasil buangan yang mengandungi nitrogen tersebut menjadi nitrogen gas semula kemudian gas nitrogen naik ke atmosfera. Proses ini dikenali sebagai kitaran nitrogen.
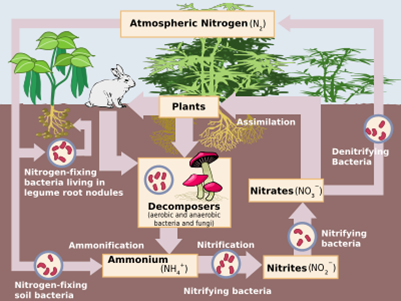
Gambarajah 1 menunjukkan proses kitaran nitrogen
Kegunaan dan aplikasi harian
1. Penghasilan Ammonia
Penggunaan nitrogen terbesar di industri adalah dalam pengeluaran ammonia (NH3). Sebahagian besar nitrogen digabungkan dengan hidrogen untuk menghasilkan ammonia melalui proses Haber. 150 juta tan ammonia dihasilkan dengan cara ini pada setiap tahun. Ammonia yang dihasilkan dalam skala yang besar kebanyakannya diguna untuk menghasilkan baja, bahan letupan, pewarna dan nitrik asid pula dihasilkan melalui proses Ostwald.
2. Penyejukkan
Cecair nitrogen juga sering digunakan sebagai bahan pendingin kerana ia mempunyai kapasiti suhu yang sangat sejuk sehingga mampu mencecah -80 °C yang selalu digunakan untuk tujuan pemeliharaan sampel biologi seperti sel DNA yang bagi tujuan penyelidikan perubatan atau kajian saintifik.
Ia juga digunakan untuk tujuan pembekuan dan mengawet makanan dengan cepat demi menjaga kelembapan, warna, rasa dan tekstur.
3. Industri Elektronik
Gas nitrogen sebahagian besarnya adalah lengai dan sesuai digunakan sebagai pelindung dalam industri semikonduktor semasa proses kimpalan dan pematerian dijalankan. Ia juga digunakan dalam industri elektronik seperti pembuatan transistor dan diod. Nitrogen juga digunakan dalam kuantiti yang besar untuk memudahkan proses penyepuhlindapan keluli tahan karat. Selain itu, syarikat minyak juga menggunakan gas nitrogen dengan tekanan yang tinggi untuk mengeluarkan minyak mentah ke permukaan bumi.
Unsur yang lain
Rujukan: